MRSA(メチシリン耐性黄色ブドウ球菌)はセファゾリン(CEZ)などの抗菌薬が効きづらくなった黄色ブドウ球菌の総称です。
黄色ブドウ球菌自体は非常にありふれた菌で、皮膚や鼻の粘膜、口腔内、消化管、傷口などに付着している常在菌ですが、抵抗力の弱った患者さん(大手術直後の患者、血管内にカテーテルが挿入されている患者、長期間の抗菌薬使用患者、抗がん剤使用患者、免疫不全患者など)に対して、敗血症や髄膜炎、心内膜炎、骨髄炎などを引き起こし、死亡に至ることも少なくありません。
今回はそんなMRSA感染症に使用される薬についてお話ししていきたいと思います。
抗MRSA薬一覧
| 一般名 | 商品名 | 英名 | 略 |
| バンコマイシン | バンコマイシン | Vancomycin | VCM |
| テイコプラニン | タゴシッド | Teicoplanin | TEIC |
| ダプトマイシン | キュビシン | Daptomycin | DAP |
| リネゾリド | ザイボックス | Linezolid | LZD |
| テジゾリド | シベクトロ | Tedizolid | TZD |
| アルベカシン | ハベカシン | Arbekacin | ABK |
基本はバンコマイシン(VCM)
基本的にはVCMが第一選択とされ、最も多く使用されています。
これは、MRSA感染症に対する使用経験とエビデンスが豊富であること、他の抗MRSA薬と比較して安価であることに由来します。
また、ある一定の使用基準を設けて抗MRSA薬を使用していくことで、不用意な耐性菌(特にVCM以外)を増やしたくないという感染症学的な治療戦略とも合致します。
価格比較 ※ 2022年2月時点の代表的製剤(ジェネリック)の価格として計算
- バンコマイシン(VCM):1~6V/日×681円=681~4,086円/日
- ダプトマイシン(DAP):1~2V/日×13,776円=13,776~27,552円/日
- リネゾリド(LZD):2V/日×7,414円=14,828円/日
抗MRSA薬の選択
とは言え、抗MRSA薬はVCMだけではありません。
近年、VCMが効きづらい低感受性株が少しずつではあるが増えているという問題(MIC creep)であったり、移行性が低いことやバイオフィルム感染症に対する効果の限界が指摘されています。
そのため、日本化学療法学会・日本感染症学会が公表している「MRSA感染症の治療ガイドライン 2019年改訂版」では、感染症の病態や基礎疾患に応じて適切に初期治療薬を選択することが推奨されています。
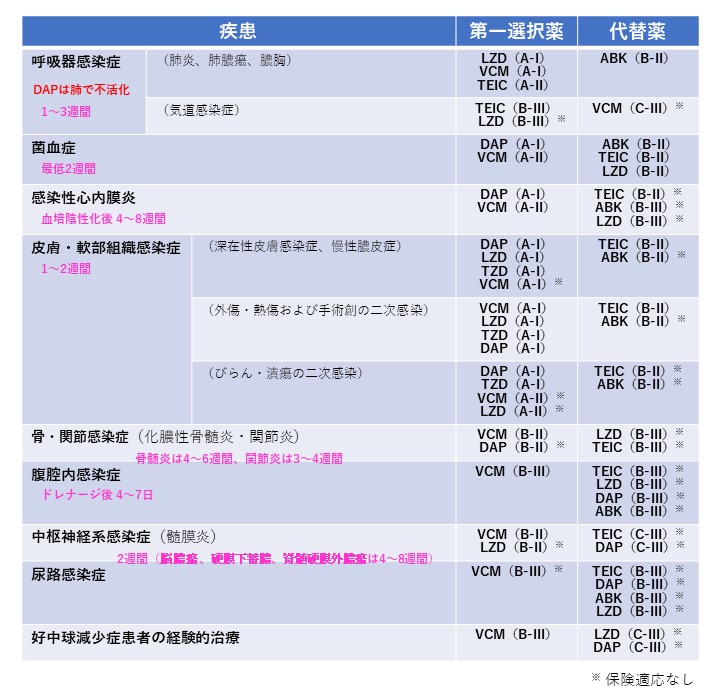
ちなみに、エビデンスレベル(A-Ⅰなど)が同じでも疾患毎に薬剤の順序が異なることに気づきましたでしょうか?
上位に記載されているものほど、推奨度が高いと言われています。
とは言え、VCM以外の薬剤を第一選択とするかについては専門家の間でも議論が分かれています。
各抗MRSA薬の特徴
バンコマイシン(VCM)
グリコペプチド系の抗菌薬で、細胞壁の合成を阻害することで効果を発揮します。
ヒスタミン遊離によるレッドマン症候群や血圧低下などの副作用が発現することがあるので、1000mgあたり60分以上の時間をかけて点滴静注します。
蛋白結合率:34.3±3.6%
組織移行性(肺組織・骨髄血・心膜液・髄液):約20~50%
組織移行性(喀痰・骨組織):約10~15%
薬物血中濃度モニタリング(TDM)
腎機能が正常(eGFR≧90mL/min/1.73m2)であれば、初回25~30mg/kg(実測体重)の負荷投与、以降1回15~20mg/kgを12時間ごとに投与し、3日目(4~5 回投与直前)にTDMを行います。
目標トラフ値は10~20μg/mLに設定し、トラフ値20μg/mL以上は腎毒性が増加するため避けます。
日本化学療法学会・日本TDM学会より「抗菌薬TDMガイドライン2016」が公表されているので、詳細はそちらを参考にしてください。
[補足]
臨床・細菌学的効果の指標としてAUC(薬物の曝露量)/MIC(最小発育阻止濃度)≧400が推奨されるが、使用経験(エビデンス)や評価ツールが限られているため、代替指標としてトラフ値を用いる。
初期投与量の目標トラフ値が10~15μg/mLに設定してあるのは、ガイドライン通りの投与量では15μg/mL以上を達成するのが困難なことに由来します。
そのため、採血から結果判明までの時間などの自施設の状況と患者の病態を考慮して柔軟に対応していくことも必要です。
腎機能障害を有する場合の初期投与量についても同様で、理論的に腎機能が悪ければ悪いほど定常状態に達するまでの時間が延長することは間違いなく、自施設の状況と患者の病態を正しく評価・判断していただければと思います。
テイコプラニン(TEIC)
VCMと同じく、グリコペプチド系の抗菌薬です。
VCMと比較して治療域が広く安全に使用できると言われていますが、使用経験(エビデンス)や評価ツール(TDM解析支援ソフト)が限られていることから、標準治療としては使用されないことが多いです。
また、現在米国では使用できないこともエビデンスが限られている原因の一つです。
蛋白結合率:90%以上(血清アルブミンの影響を受けやすい)
組織移行性:心臓や肺組織、骨は良好だが、髄液は不良です。
薬物血中濃度モニタリング(TDM)
半減期が長い(約60時間)ため負荷投与は必要不可欠です。
負荷投与として1回400mg(6mg/kg)~800mg(12mg/kg)1日2~3回を1~3日投与し、以降は約半量に減量、投与4日目のトラフ値を確認します。
トラフ値は15~30μg/mL(重症例や複雑性感染症では20μg/mL以上)を目標とし、血小板減少や腎障害を予防するため40~60μg/mL以下とします。
ダプトマイシン(DAP)
環状リポペプチド系の抗菌薬で、細胞膜の脱分極を引き起こすことで効果を発揮します。
菌血症および心内膜炎で第一選択として使用されますが、肺胞のサーファクタントで不活化されるため、呼吸器感染症では使用できないことに注意が必要です。
副作用として横紋筋融解症があるため、CPK(クレアチニンホスホキナーゼ)をモニターする必要があります。
菌血症には6mg/kg、皮膚・軟部組織感染症には4mg/kgを1日1回30分間で点滴静注します。
米国では1回8mg~10mg/kg(重症感染)に増量可能とされており、患者さんの状態に応じて投与量を選択していくことも必要です。
蛋白結合率:83.5~87.6%
移行性:髄液以外は良好(遊離型薬物濃度)
リネゾリド(LZD)
オキサゾリジノン系の抗菌薬で細菌の蛋白合成を阻害します。
肺や骨に対する移行性が良好で肺炎の第一選択薬とされていますが、菌血症へは効果がVCMより劣る可能性があります。
MRSAに対してLZDは静菌的であることが障壁となり、臨床エビデンスが少ないことに注意が必要である一方で、リネゾリド耐性のMRSAは非常に少ないことはメリットの一つと言えます。
点滴静注と経口の2剤形を有し、投与量は共に投与量は1回600mgを1日2回投与します。
LZDは特に副作用(血小板減少、貧血、セロトニン症候群、視神経障害、乳酸アシドーシスなど)に注意が必要です。
基本的には腎機能に応じた投与量の調節は必要ないとされていますが、腎機能障害時(目安:CCr 30mL/min以下)には高率で血小板低下などの副作用が発現するため、1日1回への減量も考慮されます。
経口剤の生物学的利用率:ほぼ 100%
半減期:約6時間
蛋白結合率:31%
組織移行性:良好
肺胞被覆液(415%)髄液(160%)皮膚(104%)筋肉(94%)骨(60%)
テジゾリド(TZD)
リネゾリドと同じオキサゾリジノン系の抗菌薬で、点滴静注と経口の2剤形あります。
2018年に製造販売承認された最も新しい抗MRSA薬で、現時点では皮膚・軟部組織感染症しか適応がありませんが、LZDと比較して血小板減少などの骨髄機能不全が少なく安全性が高いことが期待されています。
投与量は1回200mgを1日1回投与します。
アルベカシン(ABK)
抗MRSA薬で唯一のアミノグリコシド系の薬剤であり、細菌の蛋白合成を阻害することで効果を発揮します。
この薬も第一選択として選択されることは稀です。
組織移行性:胸水や腹水、心嚢液、滑膜液は良好ですが、髄液や皮下組織、骨は不良です。
薬物血中濃度モニタリング(TDM)
通常5.5~6.0mg/kg(約300mg)を1日1回30分かけて点滴静注し、2回目以降の投与時に血中濃度を測定します。
臨床・細菌学的効果の指標はCpeak(ピーク濃度)/MICと相関し、腎毒性はトラフ値と相関します。
Cpeakとは、点滴終了直後の最も高い血中濃度を最高血中濃度(Cmax)ではなく、組織への分布が完了(血液-組織間濃度が平衡状態)した時点で、点滴終了30分後の濃度のことです。
目標Cpeak/MIC:15~20μg/mL
目標トラフ値:1~2μg/mL未満
さいごに
今回はMRSA感染症に対する治療薬についてお話しさせていただきました。
状況に応じてスルファメトキサゾール・トリメトプリム(ST合剤)やミノマイシン(MINO)、リファンピシン(RFP)、クリンダマイシン(CLDM)なども使用されることがありますが、議論が分かれるところなので今回は割愛しています。
また、感受性良好な黄色ブドウ球菌(MSSA)に対しては、VCMよりセファゾリン(CEZ)の方が予後が良いとされていますので、エンピリック治療として抗MRSA薬を始めたとしても、しっかりとデ・エスカレーションすることが大事です。
保菌だけで発症していなければ治療の対象とならないことも覚えておきましょう。
ちなみに、MRSAは基本的に接触により感染が伝播するため、手指衛生や環境消毒による接触感染予防策が有用です。